  |
| Politica de confidentialitate |
|
|
| • domnisoara hus • legume • istoria unui galban • metanol • recapitulare • profitul • caract • comentariu liric • radiolocatia • praslea cel voinic si merele da aur | |
Intoxicatii cu etilen glicol, propilen si dietilen glicol si metanol
1.Intoxicatia cu etilen glicol
Definitie
Etilen glicolul (monoetilen glicol (MEG), dupa IUPAC: etan-1,2-diol) este un alcool cu doua grupari -OH (un diol) utilizat in lumea larga ca antigel auto.In forma sa pura,este un lichid indor, incolor, siropos si cu un gust dulce.
MEG este toxic, iar ingestia sa trebuie considerata o urgenta medicala.
Istoric
Etilen glicolul a fost prima data preparat in anul 1856 de catre chimistul francez Charles-Adolphe Wurtz


Acesta s-a nascut in Wolfisheim, langa Strasbourg, si a studiat la Strasbourg. In 1844 s-a mutat la Paris si a lucrat in Sorbonne, unde a devenit professor in 1874.
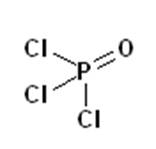
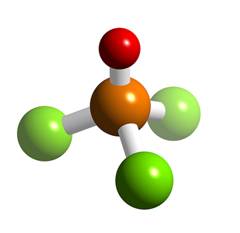
Wurtz initial a lucrat la oxizii si oxiacizii fosforului, iar in anul 1846 a descoperit oxiclorura de fosfor (POCl3).
In 1855, acesta a descoperit o metoda de a sintetiza hidrocarburile prin tratarea halogenurilor de alchil cu sodiu (cunoscuta si astazi drept Reactia Wurtz)., mecanismul acestei reactii fiind:
Un electron de la sodiu este transferat la halogen pentru a forma o halogenura de sodium si un radical alchil.
R-X + Na → R. + Na+X−
Radicalul alchil accepta apoi un electron de la un alt atom de sodiu pentru a forma un anion alchil si astfel sodiul devine cationic.
R. + Na → R−Na+
Apoi anionul alchil inlocuieste halogenura, formand o noua legatura covalenta carbon-carbon.
R−Na+ + R-X → R-R + Na+X−
Exemplu:
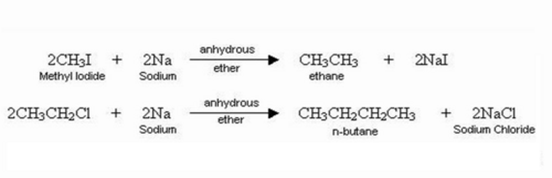
In 1856 a descoperit glicolii, iar oxidarea acestora, l-au condus pe Wurtz la omologii acidului lactic. De asemenea, a preparat neurina sintetic,in 1867, prin actiunea trietilaminei asupra glicol-clorhidrinei.
Tot in acelasi an, alaturi de chimistul german Friedrich Kekulé a sintetizat fenolul din benzen.
In 1872 a descoperit aldolul , aratand dublul sau caracter: ca alcool si ca aldehida.
In anul 1880 a devenit vice-presedintele iar in 1881 presedintele Academiei, in care intrase in 1867 in succesiunea lui Théophile-Jules Pelouze.
Caracteristici
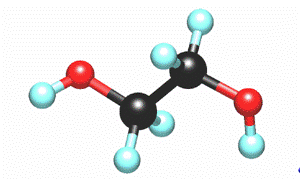
Denumire chimica: Etan-1,2-diol.
Alte denumiri: Etilen glicol, Monoetilen glicol, MEG, 1,2-etandiol.
Formula chimica: C H (0H)
Masa moleculara: 62.068 g/mol.
Densitate: 1.1132 g/cm
Vascozitate: 173 mPa. la 20°C.
Solubilitate: solubil in apa.
Punct de topire: −12.9 °C (8.8°F).
Punct de fierbere: 197.3 °C (387°F).
Etilen glicolul este produs din etilen, prin intermediul oxidului de etilen.
Oxidul de etilen reactioneaza cu apa, rezultand etilen glicolul, conform reactiei:
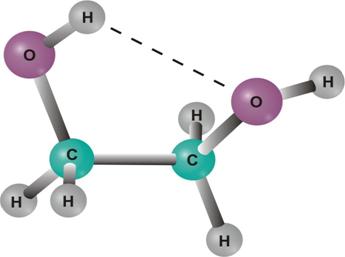
Aceasta reactie poate fi catalizata de acizi sau baze, sau poate avea loc la un pH neutru la temperature ridicate.
Cea mai mare productie de etilen glicol are loc la pH acid sau neutru, cu o cantitate crescuta de apa. In aceste conditii, se poate obtine o productie de etilen glicol in proportie de 90%.
Produsele secundare majore ale etilen glicolului sunt reprezentate de:
Dietilen glicol: C4H10O3
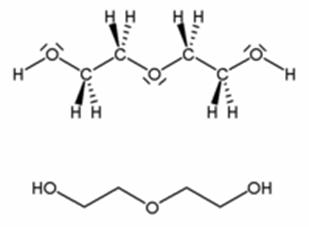
Trietilen glicol: HOCH2CH2OCH2CH2OCH2CH2OH
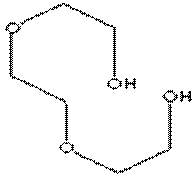
Tetraetilen glicol HO-CH2-CH2(O-CH2-CH2)3-OH
Pentaetilen glicol HO-CH2-CH2(O-CH2-CH2)4-OH
Utilizari
Etilen glicolul este utilizat ca lichid de racire sau antigel mai ales in industria auto. Datorita punctului sau scazut de inghet, este folosit de asemenea si ca lichid pentru dezghetarea parbrizelor de la automobile sau avioane. Acesta a devenit important si in industria plasticelor pentru fabricarea fibrelor de poliester, inclusiv tetraftalatul de polietilena (PET), utilizat in fabricarea sticlelor de plastic pentru bauturile nealcoolice.
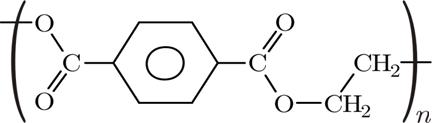 -PET
-PET
Alte utilizari:
-in fabricarea condensatoarelor

-ca intermediar chimic in productia 1,4-dioxanului.
-ca aditiv, pentru a preveni cresterea algelor in sistemul de racire al calculatoarelor.
 - Alga verde,
microscop.
- Alga verde,
microscop.
In proportie de 1-2%, etilen glicolul este folosit ca ingredient pentru cremele de pantofi, unele tipuri de cerneala si vopsea.
In unele cazuri, s-a folosit preventiv sau chiar pentru tratarea lemnului impotriva mucegaiului sau fungilor.De asemenea, este unul din putinele tratamente care au success impotriva mucegaiului la lemnul barcilor, si este relativ ieftin.
Toxicitate
Etilen glicolul reprezinta un pericol major atat pentru om (in special copiii) cat si pentru animale, avand o toxicitate crescuta consecutiv ingerarii acestuia. Datorita gustului sau dulce se pot consuma cantitati foarte mari care, deseori sunt fatale.
In tarile dezvoltate, un agent amarui denumit denatonium/denatonium benzoat, este in general adaugat etilen glicolului pentru a preveni ingestia accidentala.
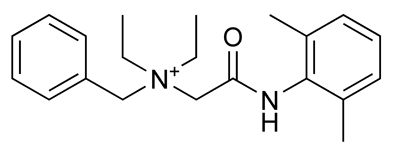 = Cation Denatonium
= Cation Denatonium
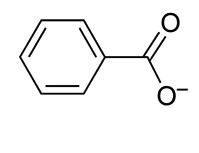 =Anion benzoate
=Anion benzoate
Desi MEG poate fi absorbit prin inhalare sau prin intermediul pielii, volatilitatea scazuta si absorbtia cutanata de asemenea scazuta, reduc probabilitatea intoxicatiilor pe aceste cai.



Simptome
Simptomele intoxicatiei cu etilen glicol, de regula, se desfasoara in trei etape:
Prima faza incepe dupa 30 minute pana la 12 ore de la ingestie iar semnele clinice sunt asociate cu sistemul nervos central.
Majoritatea animalelor prezinta seme clinice asemanatoare cu intoxicatia cu alcool, incluzand: ameteala, agitatie, dureri de cap, nistagmus, greata, diaree, tensiune crescuta.
In timp, organismul metabolizeaza etilen glicolul in alte toxine, in primul rand fiind metabolizat in glicoaldehida, care apoi este oxidata rezultand acidul glicolic, apoi acidul glioxilic, si in final acid oxalic.
S-a demonstrat ca, metabolitii toxici ai aldehidei depreseaza SNC, precum si sistemul respirator, altereaza metabolismul serotoninei si concentratia aminelor in SNC.
Faza a doua are loc la aproximativ 12-24 ore dupa ingestie si se caracterizeaza prin simptome cardio-respiratorii: dispnee, tahicardie, cianoza, hipertensiune.
A treia etapa a intoxicatiei are loc la 24-72 ore din momentul ingestiei si sunt caracteristice simptomele renale: oligourie, insuficienta renala cu anorexie, azotemie sau uremie.
Acidul oxalic rezultat din metabolismul etilen glicolului, se combina cu calciul din sange, formand astfel oxalatul de calciu.
In timp ce rinichiul incearca sa il filtreze, pH-ul tubilor renali scade, favorizand precipitarea cristalelor de oxalat de calciu.
*Datorita utilizarii sale, intoxicatia cu etilen glicol este mai frecventa* *la animalele mici.*
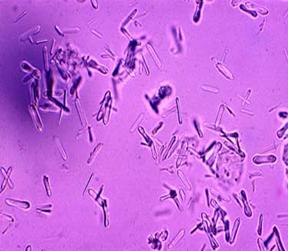
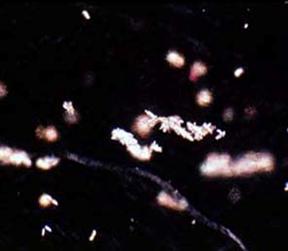
Cristale de oxalat de calciu in sedimentul Cristale de oxalate de calciu observate la
urinar la un caine intoxicat cu etilen glicol. lumina polarizata. Amprenta renala .
Cristalele de oxalat pot fi detectate in sedimentul urinar la aproximativ 3-5 ore de la ingestie.
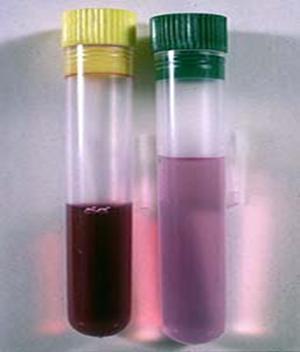
Pentru a determina concentratia de etilen glicol din sange se pot face teste colorimetrice. Aceste teste detecteaza insa numai prezenta MEG nu si a metabolitilor sai.
Test pozitiv (culoarea roz) la prezenta etilen glicolului in sange la caine la 12 ore de la ingestia toxicului.
Tratament
Consecutiv ingestiei, metabolitii etilen glicolului sunt responsabili de producerea toxicozei. Prin urmare, un prim pas in tratarea acestei intoxicatii este reprezentat de impiedicarea formarii metabolitilor, eventual in primele opt ore de la ingestie, pentru a asigura o sansa mare de supravietuire.
Primul pas metabolic care duce la toxicoza este oxidarea etilen glicolului in glicoaldehida prin intermediul alcool dehidrogenazei. Daca aceasta reactie este impiedicata, atunci etilen glicolul va fi excretat de rinichi sub forma sa initiala, fara a leza tubii renali.
Etanolul a fost folosit ca tratament standard pentru intoxicatiile cu etilen glicol. Deoarece alcool dehidrogenaza are o afinitate crescuta pentru etanol, administrarea acestuia va inhiba metabolismul MEG.
Atat etilen glicolul cat si etanolul depreseasa SNC si actioneaza ca agenti osmotici , provocand diureza. Astfel, tratamentul pe baza de etanol nu este lipsit de riscuri.
Un tratament mai modern pentru intoxicatiile cu MEG este reprezentat de administrarea 4-Metilpirazol (4-MP), ce actioneaza ca inhibitor al alcool dehidrogenazei. S-a demonstrate ca acest medicament este cel mai efficient inhibitor al metabolismului MEG, minimalizand in acelasi timp efectele toxice produse de acesta.
Cu cat timpul dintre ingestie si inceperea tratamentului creste, cu atat prognosticul devine mai rezervat.
Doza letala la caine- 4,4- 6,6 mg/kg
Doza letala la pisica- 1,4- 1,5 mg/kg
Tratamentul intoxicatiilor cu etilen glicol s-a imbunatatit pe parcursul anilor. Totusi, intoxicatia cu acest chimic, reprezinta inca o problema majora pentru medicina animalelor mici.
De aceea, prevenirea expunerii la acest toxic este cea mai buna cale pentru siguranta tuturor animalelor.


2.Intoxicatia cu propilen glicol
Definitie
Propilen glicolul, cunoscut si sub numele de propan-1,2-diol, este un lichid uleios, indor, incolor si insipid, hygroscopic si miscibil in apa, acetone si cloroform. Este fabricat prin hidratatrea oxidului de propilen.
Caracteristici
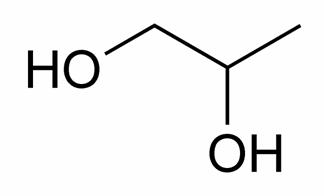
Denumire chimica: propan-1,2-diol.
Alte denumiri: propilen glicol.
Formula chimica: C H
Masa moleculara: 76.09 g/mol.
Densitate: 1.036 g/cm
Punct de topire: -59 °C.
Punct de fierbere: 188.2 °C.
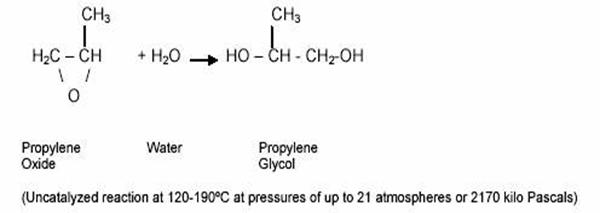
Utilizari
Ca umectant pentru medicamente, cosmetice, mancare, si
produse din tutun.




Ca lubrifiant medical si sexual.


Ca solvent pentru colorantii alimentari.
Ca aditiv alimentar, etichetat E 1520.


Ca antigel (non- toxic).



Pentru masinile de facut fum- producerea fumului artificial necesar pentru antrenamentul pompierilor si piese de teatru.


Pentru lotiuni antibacteriene si solutii saline.



Toxicitate
Utilizarea propilen glicolului in industria alimentara, cosmetica si farmaceutica este permisa in anumite cantitati, acestea fiind considerate nedaunatoare.
Propilen glicolul induce mai putine efecte adverse fata de etilen glicol, atat la oameni cat si la animale.


Toxicitatea orala a propilen glicolului este scazuta si de aceea, este recunoscut ca sigur pentru utilizrea sa directa ca aditiv alimentar.
Intr-un studiu realizat pe sobolani, carora li s-a administrat in hrana pana la 5% propilen glicol timp de 104 saptamani, s-a demonstrat ca acestia nu au dezvoltat semne de boala.
Efecte clinice
Ingestie
Simptomatologia este dependenta de doza- somnolenta, inconstienta chiar si coma.
Alte semne- hiperosmolaritatea limfei, acidoza lactica, si hipocalcemie.
Contactul cu pielea
Absorbtia cutanata este scazuta, dar poate deveni importanta in cazul in care exista leziuni la acest nivel. Efecte- iritatii locale si hipersenzitivitate.
Expunere parenterala
Propilen glicolul poate cauza- hipotensiune, bradicardie, acidoza lactica si aritmie. Consecutiv administrarii intravenoase poate produce hemoliza.
Inhalare
Nu au fost raportate efecte respiratorii, insa in cazul intoxicatiilor severe, pot avea loc tulburari respiratorii datorate deprimarii SNC.
Tratament
Dupa expunerea la doze mari, este necesara monitorizarea functiilor vitale. Din moment ce metabolitii PG sunt mai putin toxici, inhibarea metabolismului acestuia cu etanol sau 4-metil pirazol , nu este necesara.
Se recomanda lavajul gastric si inducerea vomei.
3.Intoxicatia cu dietilen glicol
Definitie
Dietilen glicolul (DEG) este un lichid indor, higroscopic, miscibil in apa si solventi organici polari precum alcooli si eteri.
Caracteristici
Denumire chimica 2-hidroxietoxi)etan-2-ol.
Alte denumiri: dietilen glicol, etilen diglicol, diglicol, 2,2'-oxibisetanol,
3-oxa-1,5-pentandiol, dihidroxi dietil eter.
Formula chimica: C H
Masa moleculara: 106.12 g/mol.
Densitate: 1.118 g/cm
Punct de topire: -10.45 °C.
Punct de fierbere: 244-245 °C.
Utilizari
Ca plastifiant pentru hartie, intra in compozitia dopurilor, a cleiurilor, adezivilor, folosit la legarea cartilor.
Ca stabilizator pentru dispersiile uleioase solubile.
In industria vopselurilor si a tipografiei.



Pentru vopselele pe baza de latex impotriva inghetului, ca antigel.



Ca solvent pentru separarea hidrocarburilor aromatice si parafinice.

Toxicitate
* Ingestia
In cazul ingestiei unor cantitati mici, DEG nu provoaca reactii adverse. Totusi, atunci cand are loc ingestia unor cantitati crescute,
poate induce greata, disconfort abdominal si diaree.
Expunerea excesiva duce la afectarea SNC, provoaca efecte cardiopulmonare (acidoza metabolica) , precum si insuficienta renala.
* Contactul cu ochii
Poate produce o usoara si temporara iritatie a ochilor.
* Contactul cu pielea
Considerat in general neiritant pentru suprafata cutanata.
* Inhalarea
La temperature camerei, expunerea la vaporii de DEG este minima datorita volatilitatii scazute a acestuia. In cazul in care incaperile nu sunt aerisite sau ventilate corespunzator, vaporii/aburii se pot acumula, si pot provoca iritatia cailor respiratorii, dureri de cap si
greata.
Daca intoxicatia s-a produs prin ingestie nu este recomandata inducerea vomei.
Informatii toxicologice
Doza letala la om- 1.2 g/kg
Doza letala la iepure- >2 g/kg



4.Intoxicatia cu metanol
Definitie
Metanolul, cunoscut si sub numele de alcool metilic, este cel mai simplu alcool; este un lichid volatile, incolor, inflamabil, cu un miros distinct si cu un gust mai dulce decat etanolul.
Metanolul este produs natural, in metabolismul anaerob al multor specii de bacterii. Ca rezultat, in atmosfera, exista o mica fractiune de vapori de methanol. In cateva zile, metanolul atmospheric este oxidat de catre oxigen, cu ajutorul razelor de soare, in dioxid de carbon si apa.
2 CH3OH + 3 O2 → 2 CO2 + 4 H2O
Istoric
In procesul de inbalsamare, egiptenii foloseau un amestec de subtante ce includea metanolul, pe care il obtineau din piroliza lemnului.
Totusi, metanolul pur, a fost prima data izolat in anul 1661 de catre Robert Boyle.


In anul 1834, chimistul francez Jean-Baptiste Dumas si Eugene Peligot i-au determinat compozitia de baza. De asemenea, au introdus cuvantul "metilen" in chimia organica, provenit de la grecescul methy= vin si hŷlē = lemn.


Dumas, Jean-Baptiste (1800 - 1884) Eugene Peligot (1811 - 1890)
Caracteristici
Denumire chimica: metanaol.
Alte denumiri: hidroximetan, alcool metilic, carbinol.
Formula chimica: CH3OH.
Masa moleculara: 32.04 g/mol.
Densitate: 0.7918 g/cm³.
Punct de topire: -97 °C (176 K).
Punct de fierbere: 64.7 °C (337.8 K).
Aciditate: ~ 15.5 pKa.
Vascozitate: 0.59 mPa la 20 °C.
Utilizari
Metanolul este utilizat pentru motoarele cu combustie interna, pe principiul ca nu este atat de inflamabil precum benzina.
Un dezavantaj important al acestei utilizari este actiunea sa coroziva asupra unor metale, inclusiv asupra aluminiului. Metanolul, desi este un acid slab, ataca invelisul de oxid, care protejeaza in mod normal aluminiul impotriva coroziunii.
6 CH3OH + Al2O3 → 2 Al(OCH3)3 + 3 H2O
Metanolul este utilizat pe scara larga, in producera altor chimicale:
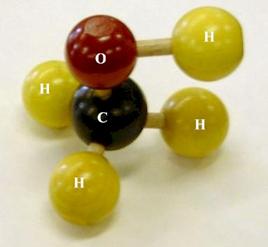
-aproape 40% din methanol este transformat in formaldehida.
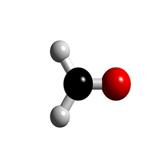
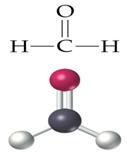
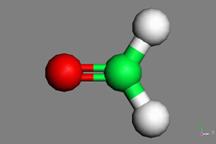
De aici, este transformat in produse diverse precum: plastice, placaje, vopsele, explozibile.




Metanolul este de asemenea folosit pentru fibrele de poliester, pentru
unii compusi din silicon, ca antigel, ca solvent pentru lichidele de spalat
parbrize. 



Toxicitate
Ca si etilen glicolul, semnele clinice in intoxicatia cu metanol, au loc in cateva ore. Desi metanolul ca atare este toxic intr-o oarecare masura, metabolitii sai sunt foarte toxici, producand acidoza, orbire, uneori moarte.
Primul pas in metabolismul metanoluli, implica enzima alcool dehidrogenaza, care oxideaza incet metanolul, producand astfel formaldehida.
Formaldehida este apoi oxidata de catre formaldehid dehidrogenaza formand acidul formic. Aceasta oxidare are loc rapid, astfel ca formaldehida se acumuleaza in cantitate mica in limfa.
In final, acidul formic este metabolizat , rezultand dioxid de carbon si apa care sunt excretate la nivelul rinichilor si plamanilor.
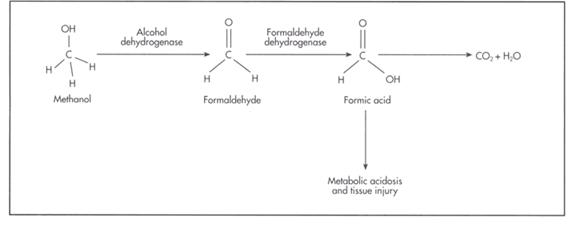
Acumularea acidului formic este responsabila pentru prezenta acidozei metabolice. De asemenea, acesta inhiba respiratia celulara, ducand la acidoza lactica.
Semne clinice
Simptomele initiale ale intoxicatiei cu metanol pot sa apara la 12 ore dupa ingestie, insa cel mai frecvent apar dupa 24 de ore.
Aceste simptome se aseamana cu cele din intoxicatia cu etanol, si includ: somnolenta, confuzie, ataxie, greata, voma, dureri abdominale. Acidoza metabolica impreuna cu efectele vizuale, reprezinta particularitatea intoxicatiei cu metanol. Disfunctiile vizuale caracteristice includ dilatatie pupilara si pierderea reflexului pupilar. Alte simptome: respiratie superficiala, cianoza, tahipnee, coma, convulsii, hipotensiune, iar in cazuri svere chiar moarte. Pacientii care supravietuiesc pot ramane cu orbire permanenta sau cu alte deficiente neurologice.
Doza toxica la caine este de 3.6 g/kg, iar la pisica aceasta doza nu a fost determinata.
La om doza toxica de metanol pur este de 1-2 ml/kg.
Tratament
Ca antidot
se foloseste alcoolul etilic, care blocheaza metabolismul alcoolului metilic si
favorizeaza eliminarea acestuia din urma din organism. La om se administreaza o
solutie de alcool etilic 50% din 4 in 4 ore, cate 0,5 ml/kg.
- Se face spalatura gastrica cu suspensie de carbune activat in solutie de
bicarbonat de sodiu 5%.
- Se provoaca voma.
- Se corecteaza acidoza.
- Hidratare intensa .
- Se aplica pansament ocluziv pe globii oculari.
- Se evita utilizarea lactatului de sodiu pentru alcalinizare si a sulfatului
de magneziu pentru combaterea edemului cerebral.







Bibliografie
Agency for Toxic Substances and Disease Registry (1997),ToxFAQS, Ethylene Glycol and Propylene Glycol (accessed, March, 1999).
Australian and New Zealand Environment and Conservation Council (ANZECC) (1992), Australian Water Quality Guidelines for Fresh and Marine Waters.
Barceloux DG, Krenzelok EP, Olson K, Watson W: American Academy of Clinical Toxicology Practice Guidelines on the Treatment of Ethylene Glycol Poisoning. Ad Hoc Committee. J Toxicol Clin Toxicol 1999
Brent J, McMartin K, Phillips S, et al: Fomepizole for the treatment of ethylene glycol poisoning. Methylpyrazole for Toxic Alcohols Study Group. N Engl J Med 1999.
Browning RG, Curry SC: Clinical toxicology of ethylene glycol monoalkyl ethers.
Burkhart K: Methanol and ethylene glycol toxicity. J Toxicol Clin Toxicol 1997.
Church AS, Witting MD: Laboratory testing in ethanol, methanol, ethylene glycol, and isopropanol toxicities.
Demey H, Daelmans R, DeBroe ME et al (1984) Propylene glycol intoxication due to intravenous nitroglycerin.
Demey HE, Daelmans R, Verpooten GA et al (1988) Propyleneglycol-induced side effects during intravenous nitroglycerin therapy. Intens Care Med.
Denning DW, Webster DB (1987) Detrimental effect of propylene glycol on natural killer cell and neutrophil function. J Pharm Pharmacol 39: 236-238.
Ellenhorn MJ and Barceloux DG. Medical Toxicology: Diagnosis and Treatment of Human Poisoning. Elsevier Publishing Co., Inc., 1998. New York. Pp. 805-809.
Hirsch DJ, et. al. A Simple Method to Estimate the Required Dialysis Time for Cases of Alcohol Poisoning. Kidney International 60: 2021-2024, 2001.
Hanif M, Mobarak MR, Ronan A, Rahman D, Donovan JJ, Bennish ML. Fatal renal failure caused by diethylene glycol in paracetamol elixir: the Bangladesh epidemic. Br Med J 1995;311:88-91.
International Programme on Chemical Safety (IPCS) (2001). Methanol. Poisons Information Monograph. PIM 335. WHO. Geneva.
International Programme on Chemical Safety (IPCS) (1997). Methanol. Environmental Health Criteria 196. WHO. Geneva.
Jacobsen D, McMartin KE (1986) Methanol and ethylene glycol poisonings. Mechanisms of toxicity, clinical course, diagnosis, and treatment. Medical Toxicology, 1:309-334.
Lamb JA, Maronpot RR, Gulati DK, Russell VS, Hommel-Barnes L, Sabharwal PS (1985) Reproductive and developmental toxicity of ethylene glycol in the mouse. Toxicology and Applied Pharmacology, 81:100-112.
Manius GJ (1979) Determination of ethylene oxide, ethylene chlorohydrin, and ethylene glycol residues in ophthalmic solutions at proposed concentration limits. Journal of Pharmacological Science, 68:1547-1549.
Maronpot RR, Zelenak JP, Weaver EV, Smith JN (1983) Teratogenicity study of ethylene glycol in rats. Drug and Chemical Toxicology, 6:579-594.
Marshall TC (1982) Dose-dependent disposition of ethylene glycol in the rat after intravenous administration. Journal of Toxicological and Environmental Health, 10:397-409.
Marshall TC, Cheng YS (1983) Deposition and fate of inhaled ethylene glycol vapor and condensation aerosol in the rat. Fundamental and Applied Toxicology, 3:175-181.
Meneghini CL, Rantuccio F, Lomuto M (1971) Additives, vehicles and active drugs of topical medicaments as causes of delayed-type allergic dermatitis. Dermatologica, 143:137-147.
Morris HJ, Nelson AA, Calvery HO (1942) Observations on the chronic toxicities of propylene glycol, ethylene glycol, diethylene glycol, ethylene glycol monoethyl ether and diethylene glycol monoethyl ether. Journal of Pharmacology and Experimental Therapeutics, 74:266-273.
NIOSH (1996) Glycols. Method 5523. In: NIOSH manual of analytical methods, 4th ed. Washington, DC, US Department of Health and Human Services, Public Health Service, Centers for Disease Control and Prevention, National Institute of Occupational Safety and Health.
NTP (1988) Developmental toxicity evaluation of ethylene glycol (CAS 107-21-1) in CD rats. Final report. Research Triangle Park, NC, Research Triangle Institute, National Institutes of Health, National Toxicology Program, 504 pp. (PB88-204326).
NTP (1993) NTP technical report on the toxicology and carcinogenesis studies of ethylene glycol (CAS Nos. 107-21-1) in B6C3F1 mice (feed studies). Research Triangle Park, NC, US Department of Health and Human Services, National Institutes of Health, National Toxicology Program, 5 pp. (NTP TR 413; NIH Publication 93-3144).
National Poisons Information Service (NPIS) (2004). Methylated Spirits. Toxbase®.
Nelson, B. K., Brightwell, W. S., MacKenzie, D. R., Khan, A., Burg, J. R., Weigel, W. W. and Goad, P. T. (1985). Teratological assessment of methanol and ethanol at high inhalation levels in rats. Fundam Appl Toxicol 5, 727-36.
Penumarthy L, Oehme FW (1975) Treatment of ethylene glycol toxicosis in cats. American Journal of Veterinary Research, 36:209-212.
Riley JH, O'Brien S, Riley MG (1982) Urine and tissue oxalate and hippurate levels in ethylene glycol intoxication in the dog. Veterinary and Human Toxicology, 24:331-334.
Storer RD, McKelvey TW, Kraynak AR, Elia MC, Barnum JE, Harmon LS, Nichols WW, DeLuca JG (1996) Revalidation of the in vitro alkaline elution/rat hepatocyte assay for DNA damage: improved criteria for assessment of cytotoxicity and genotoxicity and results for 81 compounds. Mutation Research, 368:59-101.
Tyl RW, Price CJ, Marr MC, Myers CB, Seely JC, Heindel JJ, Schwetz BA (1993) Developmental toxicity evaluation of ethylene glycol by gavage in New Zealand white rabbits. Fundamental and Applied Toxicology, 20:402-412.
Tephly TR, McMartin KE (1984). Methanol metabolism and toxicity. In: Stegink and Filer (Eds): Aspartame: physiology and biochemistry, pp. 111-140, Marcel Dekker, New York.
Tietz NW (1986). Textbook of Clinical Chemistry l68l-82. WB Saunders Company, Philadelphia.
Vale and Meredith TJ (1981). Poisoning, Diagnosis and Treatment. Update Books, London.
|
|
|
|
|
|
|